Роданид калијум је токсична супстанца која се користи у аналитичкој хемији
Роданид калијум (према модерној номенклатури ИУПАЦ-а- калијум тиоцијанат) - кристали који немају боју и мирис; у фино распршеном стању стичу бијеле боје. Супстанца има гренак акутни укус, отровна је. Калијев роданид добро се раствара у многим растварачима, као што су вода, амил алкохол и етанол.
Пријем
Супстанца се добија само хемијски,да га изолује из природних извора (крви и људске пљувачке) - је изузетно скупо. Да би се синтетисао калијум тиоцијанат, потребно је мешати растворе амонијум тиоцијаната и калијум хидроксида (тривијално име - каустични калијум).
Искуство се одвија под вучом, јерослобођени амонијак може изазвати хемијске опекотине и тровања; Затим, пречишћени раствор се филтрира и остатак упари тако да се добију кристали жељене супстанце. Када се производ пусти на 70% и довољно чиста узорак амонијум тиоцијаната, овај метод је веома ефикасан.

Други начин је осигурач сумпора са калијум-цијанидом, али овај метод добијања калијум-тиоцијаната је веома опасан због високе токсичности цијанида.
Апликација
Користе се калијум тиоцијанат, његови деривати и раствори различитих концентрација у неколико индустрија. На пример:
- Текстилна индустрија.
- Филмска фотографија.
- Органска синтеза.
- Аналитичка хемија.
Области употребе

- У текстилној индустрији. Раствор калијум-тиоцијаната се користи за обраду тканине, на пример - свиле, током обраде и обраде ради очувања првобитних својстава материјала.
- У органској синтези. Неке органске супстанце, као што су тиоуреа, синтетско уље од сенфа и различите боје, синтетишу се из калијум-тиоцијаната. Такође уз помоћ, други тиоцијанати се добијају, на пример, бакарни тиоцијанат-2.
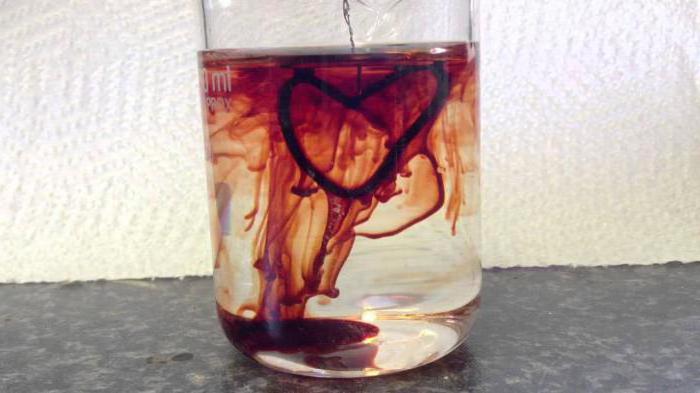
- У аналитичкој хемији, раствор калијум тиоцијанатакористи се за одређивање катиона жељеза железа у материји. Илустративни пример је реакција у којој су укључени и калијум тиоцијанат и гвожђе-3 хлорид, такође названи "крв из воде", у којој се формира црвен хексацианоферат 3; Називно име је сол с црвеном крвљу. Такође, тиоцијанати се користе за одвајање ретких метала попут торија и лантана. Калијум роданид и жељезни хлорид су недавно помогли у добијању вештачке крви за снимање, али овај метод иде у позадину због увођења рачунарске графике у филмску индустрију.
- У пољопривреди се добијају јаки инсектициди из раствора тиоцијаната. Постоје две могуће реакције:
- Први је да добије тиоциан гас уклањањем калија из соли; Родан је прилично опасан гас за све живе организме и ријетко се користи.
- Друго - распуштање калијум тиоцијаната, колекцијаослобођени током хидролизе цијанобичне киселине и оксидације добијене супстанце у цијаноген. Цијан није мање отрован, већ тежији гас у односу на шприц, па се стога често користи као инсектицид.
Калијев роданид је токсична супстанца чија смртоносна доза износи око 0,9 грама супстанце по килограму телесне тежине кад се ординише орално.
Доступност
Калијев роданид се може купити у било којој продавницихемијских реагенса, али у малим количинама због прилично високе токсичности. Просечна цена реагенса је четири стотине рубаља по килограму, а продаја је најчешће ограничена на два килограма у једној руци.
Сигурност
Због своје токсичности, калијум тиоцијанат мора се складиштити под посебним условима за сигурносне захтјеве приликом руковања отровним супстанцама:
- Кристали и раствори калијум тиоцијанат строго забрањена прогутају и веома непожељна ингресс решениј са високом концентрацијом основног супстанце на кожу.
- Упркос чињеници да је лек токсичан само упримена унутар, пожељно је радити са супстанцом у гуменим рукавицама и лабораторијским премазима, као и са свим хемијским реагенсима у складу са основним сигурносним захтјевима.
- Неопходно је изоловати супстанцу од деце и особа која немају познавање лабораторијског асистента, јер то може изазвати непријатне инциденте са губитком реагенса, неправилним примјеном и изненадном смрћу.
- Пошто је супстанца неосетљива и прилично стабилнау ваздуху, можете добити материјал за складиштење у мраку. суво ормар. Избегавајте високе влажности и директну сунчеву светлост, јер се може десити због погоршања реагенс распадања његових саставних делова. Такође стандард НФПА 704 орторомбичну етикетирање има следеће симболе: 3 0 0 В, где 3 (плаво лозенге) - токсичност, 0 (за црвене и жуте) - запаљивости и реактивности, а В - ознака за интеракцију са водом, који је ослобођен отровну тиоцијанска киселина.

И запамтите, хемијски експерименти су невероватни и јединствени, али никада не занемарујте сигурносне технике!
</ п>

